Chlorid antimoničný
Chlorid antimoničný je anorganická sloučenina s vzorcem SbCl5. Jedná se o bezbarvou kapalinu, která je ale často zbarvena do žluta. V přítomnosti vlhkosti hydrolyzuje za uvolnění chlorovodíku.
| Chlorid antimoničný | |
|---|---|
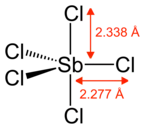
Strukturní vzorec | |

Model chloridu antimoničného | |
| Obecné | |
| Systematický název | chlorid antimoničný |
| Anglický název | Antimony(V) pentachloride |
| Německý název | Antimon(V)-chlorid |
| Sumární vzorec | SbCl5 |
| Vzhled | bezbarvá nebo červenožlutá kapalina |
| Identifikace | |
| Registrační číslo CAS | 7647-18-9 |
| PubChem | 24294 |
| SMILES | [Cl-].[Cl-].[Cl-].[Cl-].[Cl-].[SbH3+3] |
| InChI | 1S/5ClH.Sb/h5*1H;/q;;;;;+3/p-5 |
| Číslo RTECS | CC5075000 |
| Vlastnosti | |
| Molární hmotnost | 299,01 g/mol |
| Teplota tání | 2,8 °C |
| Teplota varu | 140 °C (rozklad od 106 °C) |
| Hustota | 2,336 g/cm3 (20 °C) 2,36 g/cm3 (25 °C) |
| Index lomu | 1,59255 |
| Rozpustnost v polárních rozpouštědlech |
alkoholy, kyselina chlorovodíková, sirouhlík |
| Rozpustnost v nepolárních rozpouštědlech |
tetrachlormethan |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Reakce
Chlorid antimoničný hydrolyzuje za vzniku kyseliny chlorovodíkové a oxidu-chloridu antimoničného.
- SbCl5 + H2O → SbOCl3 + 2 HCl
Tuto reakci lze potlačit vysokou koncentrací chloridů, pak vzniká komplexní anion hexachloroantimoničný:
- SbCl5 + Cl− → SbCl -
6
Vytváří řadu aduktů s Lewisovými bázemi. Má také silné oxidační vlastnosti.[2]
Využití
Využívá se jako katalyzátor polymerizací a na chloraci organických sloučenin.
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Antimony pentachloride na anglické Wikipedii.
- Antimony pentachloride. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- CONNELLY, Neil G.; GEIGER, William E. Chemical Redox Agents for Organometallic Chemistry. Chemical Reviews. 1996-1, roč. 96, čís. 2, s. 877–910. Dostupné online [cit. 2019-04-20]. ISSN 0009-2665. DOI 10.1021/cr940053x. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu chlorid antimoničný na Wikimedia Commons
Obrázky, zvuky či videa k tématu chlorid antimoničný na Wikimedia Commons
Portály: Chemie
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.

