Boyleův–Mariottův zákon
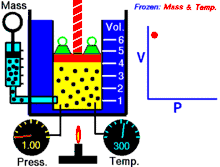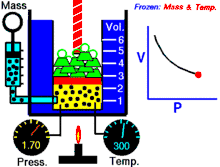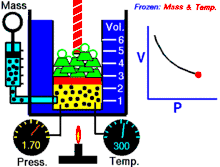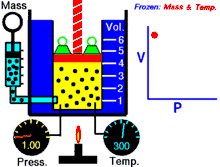
Boyleův–Mariottův zákon, zvaný též Boyleův zákon je termodynamický vztah pro izotermický děj probíhající v ideálním plynu stálé teploty.
Rovnice
Boyleův-Mariottův zákon říká, že součin tlaku a objemu plynu je stálý, tedy
- ,
kde p je tlak plynu a je objem daného množství plynu. Hodnota konstanty závisí na množství plynu a jeho teplotě a podle stavové rovnice ideálního plynu je pro danou teplotu rovna , kde n je látkové množství plynu, R je molární plynová konstanta a T je absolutní teplota plynu.
Zápis zákona se tak změní v běžně používaný tvar stavové rovnice ideálního plynu, tzn.
Vlastnosti
Boyleův-Mariottův zákon je platný pro ideální plyn. U reálného plynu však mohou (zejména při nízkých nebo naopak velmi vysokých teplotách) nastat značné odchylky od tohoto zákona, zejména vzhledem k tomu, že v ideálním plynu nejsou uvažovány žádné mezimolekulové síly (tvorba vicemolekulových komplexů při nízkých teplotách) ani změny chemického složení s teplotou (disociace molekul při vysokých teplotách. Teplota, při které se součin p.V se změnou tlaku nemění, se nazývá Boyleova teplota.)
Historická poznámka
Boyleův-Mariottův zákon formuloval roku 1662 irský přírodovědec Robert Boyle. Podle některých historiků vědy však velmi pravděpodobně jeho exaktní matematickou formulaci nevypracoval sám Boyle (vzhledem k jeho menším znalostem matematiky), ale spíše jeho asistent Robert Hooke. Ten také vyvinul vývěvu, potřebnou k experimentálnímu ověření tohoto vztahu. Nezávisle na nich dospěl ke stejnému zjištění v roce 1676 i francouzský fyzik Edme Mariotte.
Boyleův-Mariottův zákon je historicky prvním zákonem, popisující izoproces ideálního plynu (v tomto případě izotermický děj). I když se tepelnou roztažností vzduchu zabýval již Guillaume Amontons (*1663, rok po objevu Boyleova zákona), první přesné měření publikovali až v roce 1802 nezávisle na sobě Joseph Louis Gay-Lussac a John Dalton.)
Další zákony
- Gay-Lussacův zákon popisuje lineární závislost objemu ideálního plynu na jeho teplotě při konstantním tlaku – izobarický proces. Konstanta úměrnosti se nazývá teplotní objemová roztažnost při konstantním tlaku .
- Charlesův zákon říká, že tlak plynu je přímo úměrný jeho termodynamické teplotě při konstantním objemu, tudíž popisuje izochorický děj a konstanta úměrnosti se nazývá teplotní rozpínavost při konstantním objemu .
Všechny výše uvedené zákony popisují chování konstantního množství plynu. Při ději se nemění počet částic. Zákon tvrdící, že ve stejných objemech plynů při stejné teplotě a stejném tlaku je obsažen vždy stejný počet částic, se nazývá Avogadrův zákon. Konstantní počet částic v jednotkovém objemu za normální teploty a normálního tlaku je popsán Loschmidtovým číslem. V důsledku platnosti Avogadrova zákona mohla být určena molární plynová konstanta R.
Zobecněním všech uvedených čtyř zákonů spolu se znalostí plynové konstanty R bylo možné dospět k formulaci stavové rovnice ideálního plynu. Stalo se tak více než sto let po objevu Boyle-Mariottova zákona. Bylo to tím, že ve fyzice jednak trvalo poměrně dlouhou dobu, než se podařilo vůbec odlišit pojmy teplo a teplota, dlouho též trvalo dospět k pojmu absolutní teploty. Gay-Lussac, Dalton i Charles formulovali své zákony ještě v době, kdy pojem absolutní teploty nebyl znám, a proto tvar jejich zákonů měl složitější tvar než dnes. Sir William Thomson alias Lord Kelvin, který tyto věci vyřešil, se narodil až v roce 1824.
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu Boyleův-Mariottův zákon na Wikimedia Commons
Obrázky, zvuky či videa k tématu Boyleův-Mariottův zákon na Wikimedia Commons