Oxid olovnatý
Oxid olovnatý alebo glieda (v širšom zmysle)[1][2] (PbO) je binárna zlúčenina olova a kyslíka. Vyskytuje sa v dvoch polymorfoch - masikot a glieda (v užšom zmysle) (litargit). Bežným využitím oxidu olovnatého je výroba olovnatého skla, priemyselnej keramiky a počítačových komponentov.
| Oxid olovnatý | |||||||
 Oxid olovnatý | |||||||
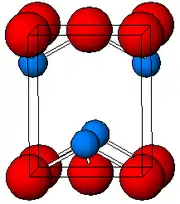 Oxid olovnatý | |||||||
| Všeobecné vlastnosti | |||||||
| Sumárny vzorec | PbO | ||||||
| Vzhľad | žltá alebo červená tuhá látka | ||||||
| Fyzikálne vlastnosti | |||||||
| Molekulová hmotnosť | 223,20 g/mol | ||||||
| Teplota topenia | 888 °C | ||||||
| Teplota varu | 1477 °C | ||||||
| Hustota | 9,53 g/cm3 | ||||||
| |||||||
| Ďalšie informácie | |||||||
| Číslo CAS | 1317-36-8 | ||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||
Výroba
Oxid olovnatý sa môže vyrobiť zohrievaním olova pri prístupe vzduchu na teplotu približne 600 °C. Pri tejto teplote je to takisto konečný produkt oxidácie ostatných oxidov olova.
- PbO2 –(293 °C)→ Pb12O19 –(351 °C)→ Pb12O17 –(375 °C)→ Pb3O4 –(605 °C)→ PbO
Tepelná dekompozícia dusičnanu olovnatého alebo uhličitanu olovnatého takisto vytvára oxid olovnatý.
- 2 Pb(NO3)2 → 2 PbO + 4 NO2 + O2
- PbCO3 → PbO + CO2
Vo veľkých množstvách sa oxid olovnatý vyrába ako medziprodukt spracovávania olovenej rudy na olovo. Bežnou olovenou rudou je galenit (sulfid olovnatý). Pri vysokých teplotách sa sulfid mení na oxid.
- 2 PbS + 3 O2 → 2PbO + 2SO2
Masikot
Oxid olovnatý sa pod názvom masikot (massicot) používa ako žltý pigment v maliarstve. V minulosti sa získaval žíhaním olovenej beloby na 300 °C. Bol jedným z najdôležitejších pigmentov od preddynastického Egypta až do konca 18. storočia.
Zdroje
- Banícky terminologický slovník. Bratislava: Vyd. SAV, 1955, S. 28 [1], S. 19, 167
- glieda. In: Malá encyklopédia chémie. 3. vyd. Bratislava : Obzor, 1981. 816 s. (Malé encyklopédie vydavateľstva Obzor.) S. 276.
