Heptán
Heptán (C7H16, presnejšie n-heptán) je za bežných podmienok kvapalným uhľovodíkom zo skupiny alkánov. S jeho pomocou je definovaná stupnica ktorá určuje oktánové číslo paliva do spaľovacích motorov.
| Heptán | |||||||||||||||||||||||||||||||||||||||
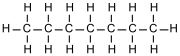 Heptán | |||||||||||||||||||||||||||||||||||||||
 Heptán | |||||||||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||||||||
| Sumárny vzorec | CH3(CH2)5CH3 (C7H16) | ||||||||||||||||||||||||||||||||||||||
| Synonymá | N-heptán | ||||||||||||||||||||||||||||||||||||||
| Vzhľad | Bezfarebná kvapalná látka | ||||||||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 100,2 u | ||||||||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 100,21 g/mol | ||||||||||||||||||||||||||||||||||||||
| Teplota topenia | −90,61 °C/183,15 K | ||||||||||||||||||||||||||||||||||||||
| Teplota varu | 98,42 °C/371,15 K (1 013 hPa) | ||||||||||||||||||||||||||||||||||||||
| Hustota | 0,684 g/cm3 | ||||||||||||||||||||||||||||||||||||||
| Rozpustnosť | vo vode: 0,22 mg/100 ml (25 °C) | ||||||||||||||||||||||||||||||||||||||
| Teplota vzplanutia | −4 °C | ||||||||||||||||||||||||||||||||||||||
| Teplota vznietenia | 285 °C | ||||||||||||||||||||||||||||||||||||||
| Medze výbušnosti | 1,1 až 6,7 % | ||||||||||||||||||||||||||||||||||||||
| Termochemické vlastnosti | |||||||||||||||||||||||||||||||||||||||
| Štandardná entropia | 328,57 J K−1 mol−1 | ||||||||||||||||||||||||||||||||||||||
| Merná tepelná kapacita | 224,64 J K−1 mol−1 | ||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||||||||
| Číslo CAS | 142-82-5 | ||||||||||||||||||||||||||||||||||||||
| Číslo UN | 1206 | ||||||||||||||||||||||||||||||||||||||
| EINECS číslo | 205-563-8 | ||||||||||||||||||||||||||||||||||||||
| Číslo RTECS | MI7700000 | ||||||||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||||||||

ADR tabuľka
Izoméry a enantioméry
Existuje deväť izomérov heptánu, prípadne jedenásť počítajúc v to aj enantioméry chirálnych zlúčenín:
- Heptán (n-heptán), CH3CH2CH2CH2CH2CH2CH3 je priamy reťazec siedmich atómov uhlíka
- 2-metylhexán (Izoheptán), CH3CH(CH3)CH2CH2CH2CH3: je priamy reťazec šiestich atómov uhlíka, s jednou metylovou skupinou na druhej pozícii
- 3-metylhexán, CH3CH2C*H(CH3)CH2CH2CH3 (chirálny): je priamy reťazec šiestich atómov uhlíka, s jednou metylovou skupinou na tretej pozícii
- 2,2-dimetylpentán (Neoheptán), CH3C(CH3)2CH2CH2CH3: je priamy reťazec piatich atómov uhlíka, s dvoma metylovými skupinami na druhej pozícii
- 2,3-dimetylpentán, CH3CH(CH3)C*H(CH3)CH2CH3 (chirálny): je priamy reťazec piatich atómov uhlíka, s jednou metylovou skupinou na druhej a tretej pozícii
- 2,4-dimetylpentán, CH3CH(CH3)CH2CH(CH3)CH3: je priamy reťazec piatich atómov uhlíka, s jednou metylovou skupinou na druhej a štvrtej pozícii
- 3,3-dimetylpentán, CH3CH2C(CH3)2CH2CH3: je priamy reťazec piatich atómov uhlíka, s dvoma metylovými skupinami na druhej pozícii
- 3-etylpentán, CH3CH2CH(CH2CH3)CH2CH3: je priamy reťazec piatich atómov uhlíka, s jednou etylovou skupinou na tretej pozícii
- 2,2,3-trimetylbután, CH3C(CH3)2CH(CH3)CH3: je priamy reťazec štyroch atómov uhlíka s dvoma metylovými skupinami na druhej a s jednou na tretej pozícii
Výskyt v prírode
Heptán sa prirodzene vyskytuje v živici stromov ako jedno z rozpúšťadiel. Veľmi vysoký obsah heptánu v živici má napr. borovica Jeffreyova z ktorej bol v minulosti izolovaný pre stanovovanie oktánového čísla. Malé množstvo heptánu sa vyskytuje napr. v silici lipy malolistej.
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Heptan na českej Wikipédii.
| Chemický portál |
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.







