Citrát trivápenatý
Citrát trivápenatý je jedna z troch vápenatých solí, kyseliny citrónovej. Bežne sa používa v potravinárskom priemysle (býva označovaný ako prídavná látka E 333 iii) ako konzervačná látka, ale niekedy aj na chuť. V tomto zmysle je podobný citrátu trisodnému. Citrát trivápenatý sa tiež používa ako zmäkčovač vody, pretože citrátové ióny dokážu chelátovať nežiaduce kovové ióny.
| Citrát trivápenatý | |||||||||||||||||||||||||||||||||||||
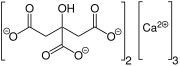 Citrát trivápenatý | |||||||||||||||||||||||||||||||||||||
| Všeobecné vlastnosti | |||||||||||||||||||||||||||||||||||||
| Sumárny vzorec | Ca3(C6H5O7)2 | ||||||||||||||||||||||||||||||||||||
| Synonymá | Citran trivápenatý Citrónan trivápenatý Trivápenatá soľ kyseliny citrónovej | ||||||||||||||||||||||||||||||||||||
| Vzhľad | Biela prášková látka | ||||||||||||||||||||||||||||||||||||
| Fyzikálne vlastnosti | |||||||||||||||||||||||||||||||||||||
| Molekulová hmotnosť | 498,5 u (bezvodý) 570,5 u (tetrahydrát) | ||||||||||||||||||||||||||||||||||||
| Molárna hmotnosť | 498,46 g/mol (bezvodý) 570,5 g/mol (tetrahydrát) | ||||||||||||||||||||||||||||||||||||
| Teplota topenia | 120 °C (dehydratácia) | ||||||||||||||||||||||||||||||||||||
| Hustota | 1,63 g/cm³ | ||||||||||||||||||||||||||||||||||||
| Rozpustnosť | vo vode: 0,085 g/100 ml (18 °C) 0,095 g/100 ml (25 °C) | ||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
| Ďalšie informácie | |||||||||||||||||||||||||||||||||||||
| Číslo CAS | 813-94-5 (bezvodý) 5785-44-4 (tetrahydrát) | ||||||||||||||||||||||||||||||||||||
| EINECS číslo | 212-391-7 | ||||||||||||||||||||||||||||||||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavy SI. Ak nie je hore uvedené inak, údaje sú za normálnych podmienok. | |||||||||||||||||||||||||||||||||||||
Chemické vlastnosti
Citrát trivápenatý je biela prášková látka bez zápachu, rozpustná v studenej vode.
Rovnako ako kyselina citrónová aj citrát trivápenatý má kyslú chuť.
Výroba
Citrát trivápenatý je medziprodukt pri izolácii kyseliny citrónovej z fermentačného procesu. Kyselina citrónová zo živného roztoku je neutralizovaná hydroxidom vápenatým, za vzniku citrátu trivápenatého. Ten sa potom odfiltruje od zvyšku vývaru a premyje. Vyrobený citrát trivápenatý môže byť predávaný tak ako je, alebo môže byť premenený na kyselinu citrónovú pomocou zriedenej kyseliny sírovej.
Biologická funkcia
U mnohých ľudí, bola zistená lepšia biologická dostupnosť citrátu trivápenatého ako u lacnejšieho uhličitanu vápenatého. Zmeny zažívacieho traktu môžu zmeniť spôsob, akým sa vápnik vstrebáva do tela. Podľa výskumu spôsobov, akým sa vstrebáva vápnik po žalúdočnom by-passe, citrát trivápenatý môže mať lepšiu biologickú dostupnosť ako uhličitan vápenatý.
Zdroj
Tento článok je čiastočný alebo úplný preklad článku Calcium citrate na anglickej Wikipédii.


