Rutherfordův experiment
Rutherfordův experiment nebo také Geigerův-Marsdenův experiment byl experiment provedený Hansem Geigerem a Ernestem Marsdenem pod vedením Ernesta Rutherforda v roce 1909 v Manchesteru. Experiment měl za cíl sledovat vnitřní strukturu atomu. Jeho neočekávané výsledky vedly k opuštění Thomsonova modelu, zvaného též pudinkový a zavedení Rutherfordova modelu.
Historie
Nejrozšířenějším modelem popisujícím atomy byl na počátku 20. století Thomsonův pudinkový model. Tento vymyslel v roce 1904 Joseph John Thomson, objevitel elektronu. Jeho model počítal se záporně nabitými elektrony, které se měly vznášet uvnitř kladně nabité homogenní koule, podobně jako hrozinky v pudinku, odtud název pudinkový model. Tento model byl ve fyzice dominantní až do roku 1911, kdy Rutherford zveřejnil výsledky svého týmu.
Experiment provedli v roce 1909 fyzik Hans Geiger a student Ernst Marsden pod dohledem vedoucího katedry fyziky na univerzitě v Manchesteru Ernesta Rutherforda.
Experiment
Rutherfordův experiment sestával ze série testů, v nichž kladně nabité alfa částice (jádra helia) bombardovaly tenký list zlaté fólie. V případě správnosti Thompsonova modelu atomu měly alfa částice pronikat fólií bez většího ovlivnění, jelikož jsou alfa částice hmotné a elektrický náboj je podle Thompsonova modelu široce distribuován. Nicméně skutečné výsledky byly pro Rutherforda překvapivé. Ačkoli mnoho alfa částic skutečně skrz fólii proniklo, řada z nich mělo velmi odkloněné dráhy a některé se dokonce odrazily a vrátily zpět ke zdroji záření.
V podrobnějším popisu byly částice záření alfa generovány radioaktivním rozpadem radonu směrem do olověného kontejneru obráceného otvorem směrem k velmi tenké zlaté fólii. Fólie pokrytá sulfidem zinečnatým byla v tomto experimentu detailně zkoumána pod mikroskopem. Mikroskop se může otáčet kolem zlaté fólie, aby bylo možné pozorovat částice, jejichž dráha byla vychýlena o stanovený úhel. Podle Thomsonova modelu by částice měly být vychýleny maximálně o několik stupňů. Nicméně bylo zjištěno, že malé procento částic je vychýleno mnohem více.
Důsledky a závěry
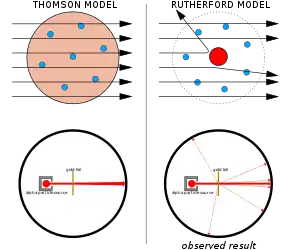
Vpravo: skutečný výsledek experimentu vedoucí k vytvoření Rutherfordova modelu atomu.
Výsledky experimentu prokázaly, že Thomsonův model atomu je neplatný. Skutečnost, že se mnoho alfa částic vychýlí o větší úhly nebo dokonce odrazí zpět ke zdroji značí, že v atomu je na malém objemu ve středu soustředěn pozitivní náboj s vysokou hmotností. Alfa částice procházející středem nebo poblíž středu atomu se srazí s kladně nabitým středem nebo s ním interagují. Vzhledem k tomu, že řada částic pronikla fólií bez ovlivnění, znamená to, že střed atomu musí být dostatečně malý ve srovnání se zbytkem.
Většina alfa částic měla odchylky nulové nebo jen velmi malé, tudíž dospěl Rutherford k závěru, že zbytek atomu je oblast s velmi nízkou hustotou. Celý kladný elektrický náboj se nachází ve velmi hmotném a hustém středu atomu, ve struktuře, které Rutherford říkal těžiště a později získala název atomové jádro. Z těchto výsledků tedy vychází dnešní představa o atomu jako o struktuře s pozitivně nabitým hustým a hmotným jádrem, kolem nějž obíhají záporné elektrony v relativně velké vzdálenosti ve srovnání s velikostí jádra.
Rutherford výsledky experimentu publikoval v roce 1911. Definitivně odmítl možnost platnosti Thomsonova modelu, jelikož žádný ze záporných elektronů nemá dostatečné množství záporného náboje nebo hmotnosti, aby ovlivnil dráhu alfa částic. Místo toho Rutherford navrhl, že uvnitř ve středu atomu se nachází kladně nabité jádro v němž je soustředěna většina hmotnosti atomu a kolem obíhají záporně nabité částice relativně daleko od jádra.
Při analýze výsledků použil Rutherford striktně Newtonovy metody klasické fyziky. Později, když se rozvinula kvantová mechanika, bylo zjištěno, že její metody dávají v tomto případě stejné výsledky jako ty odvozené Rutherfordem klasickými metodami.
Ačkoli měl Rutherfordův model atomu řadu problémů, například s distribucí náboje elektronu a další, které byly vyřešeny nástupem kvantové mechaniky, hlavní závěr experimentu, existence atomového jádra, je platný i v 21. století.
Rutherfordův model atomu byl v roce 1913 vylepšen Nielsem Bohrem. Přestože i Bohrův model atomu byl brzy nahrazen kvantově mechanickým modelem atomu, Bohrův model se i na začátku 21. století pro mnoho fyzikálních účelů používá jako přijatelné zjednodušení. Rutherfordovy výsledky přinesly základ pro všechny budoucí modely atomu a pro budoucí vývoj jaderné fyziky.
Reference
V tomto článku byl použit překlad textu z článku Eksperyment Rutherforda na polské Wikipedii.
Externí odkazy
 Obrázky, zvuky či videa k tématu Rutherfordův experiment na Wikimedia Commons
Obrázky, zvuky či videa k tématu Rutherfordův experiment na Wikimedia Commons