RECQ4
Gen lidské RECQ4 helikázy byl identifikován v roce 1998 a lokalizován na dlouhém raménku (q) chromozomu 8 v pozici 24.3.[1] Gen RECQ4 je složen z 21 exonů a 13 intronů zahrnující 6 kb genomické DNA.[2]
Proteinový řetězec RECQ4 je kódován 1208 aminokyselinami s molekulovou hmotností 133 kDa zahrnující ve svém centru vysoce konzervovanou helikázovou doménu typickou pro členy RecQ rodiny. Nicméně, ve srovnání s ostatními RecQ helikázami RECQ4 postrádá RQC a HRDC domény zodpovědné primárně za vazbu k DNA. Na druhou stranu N-terminální část RECQ4 vykazuje vysokou homologii s proteinem Sld2, který je velmi důležitý pro začátek DNA replikace u kvasinek. Předpokládá se, že tato Sld2 doména by mohla určovat roli RECQ4 v průběhu replikace DNA v lidských buňkách. [3] C-terminální část RECQ4 nebyla dosud[kdy?] řádně charakterizována.
Biochemická charakterizace RECQ4
Při první biochemické charakterizaci RECQ4 nebyla pozorována žádná helikázová aktivita tohoto proteinu in vitro.[4] Později[kdy?] bylo prokázáno, že RECQ4 vlastní helikázovou aktivitu, která je velmi nízká a substrátově specifická (tj. RECQ4 je schopen rozvíjet pouze krátké DNA vidlice s délkou komplementární části pouze 11 bp).[5] Kromě helikázové aktivity se RECQ4 protein vyznačuje také velmi silnou schopností nasedání komplementárních úseku ssDNA do dvoušroubovice[4] N-terminální část RECQ4 přímo interaguje s proteinem MCM10, který zprostředkovává spojení RECQ4 s MCM2-7. MCM2-7 komplex zastává úlohu hlavní helikázy rozplétající dsDNA při DNA replikaci a tím se RECQ4 stává nedílnou součástí MCM replikačního helikázového komplexu účastnícího se DNA replikace v lidských buňkách.[6] Další publikace pak ukazují, že RECQ4 má také nepostradatelnou roli při opravě poškozené DNA. Protein RECQ4 by se mohl pravděpodobně podílet na správném průběhu NER, a to zejména díky interakci s proteinem XPA (Xeroderma pigmentosum skupina A).[2] Navíc, bylo prokázáno, že protein RECQ4 by mohl mít funkci při udržování telomer, které fungují také jako mechanická ochrana na koncích lineárních eukaryotických chromozomů.[7] Další studie pak naznačují, že RECQ4 se akumuluje v mitochondriích a fyzicky interaguje s proteinem p53 – významným tumorovým supresorem.[8] Je také velmi pravděpodobné, že RECQ4 by mohl mít úlohu při opravě DSB pomocí HR, protože interaguje s proteinem RAD51 – klíčovým faktorem v HR.[9]
I navzdory mnoha studiím a publikacím o RECQ4, zůstává tento protein nejméně charakterizovaným členem RecQ rodiny. Stále není jasné, jaká je jeho přesná role a jaký je mechanismus jeho funkce v metabolismu DNA. Navíc, pochopení jeho funkce při replikaci a opravě poškozené DNA je nezbytně důležité pro potenciální objasnění molekulární podstaty syndromů, které vznikají díky mutacím v jeho genu. Mutace v genu RECQ4 jsou spojeny se třemi velmi zákeřnými dědičnými onemocněními: syndromem RAPADILINO, Rothmund-Thomsonovým syndromem a Baller-Geroldovým syndromem.
Syndromy spojené s RECQ4 proteinem
Rothmund-Thomsonův syndrom
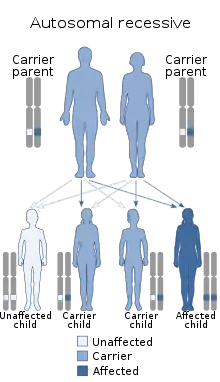
RTS je autosomálně recesivní onemocnění s charakteristickou červenou vyrážkou (poikiloderma) a různorodými klinickými projevy zahrnující malý vzrůst, šedý zákal, kosterní defekty a abnormality. Mezi těžší projevy syndromu pak patří předčasné stárnutí a predispozice k rakovině kostí (osteosarkoma).[10] RTS byl poprvé popsán již v roce 1969 německým oftalmologem Augustem von Rothmunden, který sledoval pacienty s poikilodermou, růstovou retardací a rapidně postupujícím šedým zákalem.[11]
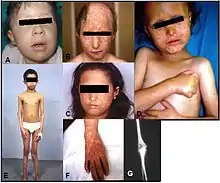
V roce 1936 britský dermatolog Matthew Sydney Thomson informoval o třech pacientech s poikilodermou, růstovou retardací a skeletárními defekty, bez známky šedého zákalu [12].Název Rothmund-Thomsonův syndrom poprvé použil Dr. William Taylor v roce 1957 k popsání skupiny pacientů s výše zmíněnými klinickými příznaky.[10] Mutace v genu RECQ4 byly prokázány u 40–66 % pacientů.[13] Při zkoumání spojitosti mezi ostesarkomou a mutacemi RECQ4 genu, bylo prokázáno, že 100 % pacientů má alespoň jednu zkracující (nonsense) mutaci.[10]
RAPADILINO syndrom
RAPADILINO (= znaky charakterizující toto onemocnění: RAdial hypo/-aplasia (radiální hypoplazie/aplazie), PAtellae hypo-/aplasia(patelární hypoplazie/aplazie) and cleft or highly arched PAlate (rozštěp nebo vysoké patro), DIarrhoea (průjem) and DIslocated joints (dislokované klouby), LIttle size (malý vzrůst) and LImb malformation (malformace končetin), NOse slender (útlý nos) and NOrmal intelligence (normální inteligence) syndrom byl poprvé popsán v roce 1989 Kääriäinenem et al. Pacienti trpící tímto syndromem vykazují společné znaky s RTS pacienty, a to poruchy růstu, deformace kostí, hlavně špatný vývoj kostí v předloktí a palce. Na rozdíl od RTS pacientů poikiloderma se u RAPADILINO pacientů nevyskytuje. Nejvíce RAPADILINO pacientů bylo identifikováno ve Finsku, s menším počtem případů se pak můžeme setkat v jiných populacích-[13][14]
Ballerův-Geroldův syndrom
BGS byl poprvé popsán Ballerem a Gerold informoval o prvních pacientech s radiální hypoplazií spojenou s kraniosynostózou. BGS má mnoho znaků překrývajících se s RAPADILINO a RTS syndromem, nicméně se nevyznačuje poikilodermou ani zvýšeným rizikem osteosarkomy. Na rozdíl od ostatních RECQ4 syndromů lidé s BGS trpí kraniosynostózou ve spojení s radiální aplazií.[15]
Reference
- [Kitao S, Ohsugi I, Ichikawa K, Goto M, Furuichi Y, Shimamoto A. Cloning of two new human helicase genes of the RecQ family: biological significance of multiple species in higher eukaryotes. Genomics 1998, 54: 443-452]
- [Fan W, Luo J. RecQ4 facilitates UV light-induced DNA damage repair through interaction with nucleotide excision repair factor xeroderma pigmentosum group A (XPA). J Biol Chem 2008, 283: 29037-29044]
- [Chu WK, Hickson ID. RecQ helicases: multifunctional genome caretakers. Nat Rev Cancer 2009, 9: 644-654]
- [Macris MA, Krejci L, Bussen W, Shimamoto A, Sung P. Biochemical characterization of the RECQ4 protein, mutated in Rothmund-Thomson syndrome. DNA Repair (Amst) 2006, 5: 172-180]
- [Suzuki T, Kohno T, Ishimi Y. DNA helicase activity in purified human RECQL4 protein. J Biochem 2009, 146: 327-335]
- [Xu X, Rochette PJ, Feyissa EA, Su TV, Liu Y. MCM10 mediates RECQ4 association with MCM2-7 helicase complex during DNA replication. EMBO J 2009, 28: 3005-3014]
- [Ghosh AK, Rossi ML, Singh DK, Dunn C, Ramamoorthy M, Croteau DL, Liu Y, et al. RECQL4, the protein mutated in Rothmund-Thomson syndrome, functions in telomere maintenance. J Biol Chem 2012, 287: 196-209]
- [Sengupta S, Shimamoto A, Koshiji M, Pedeux R, Rusin M, Spillare EA, Shen JC, et al. Tumor suppressor p53 represses transcription of RECQ4 helicase. Oncogene 2005, 24: 1738–1748]
- [Petkovic M, Dietschy T, Freire R, Jiao R, Stagljar I. The human Rothmund-Thomson syndrome gene product, RECQL4, localizes to distinct nuclear foci that coincide with proteins involved in the maintenance of genome stability. J Cell Sci 2005, 118: 4261-4269]
- [Larizza L, Roversi G, Volpi L. Rothmund-Thomson syndrome. Orphanet J Rare Dis 2010, 5: 2]
- [Rothmund Av. Über Cataracten in Verbindung mit einer eigenthümlichen Hautdegeneration. ed.: Arch.Ophthalmol. 1868: 159-182]
- [Thomson MS. A hitherto undescribed familial disease. ed.: Br. J. Dermatol. 1923: 455-462]
- [Siitonen HA, Sotkasiira J, Biervliet M, Benmansour A, Capri Y, Cormier-Daire V, Crandall B, et al. The mutation spectrum in RECQL4 diseases. Eur J Hum Genet 2009, 17: 151-158]
- [Siitonen HA, Kopra O, Kääriäinen H, Haravuori H, Winter RM, Säämänen AM, Peltonen L, et al. Molecular defect of RAPADILINO syndrome expands the phenotype spectrum of RECQL diseases. Hum Mol Genet 2003, 12: 2837–2844]
- [Van Maldergem L, Siitonen HA, Jalkh N, Chouery E, De Roy M, Delague V, Muenke M, et al. Revisiting the craniosynostosis-radial ray hypoplasia association: Baller-Gerold syndrome caused by mutations in the RECQL4 gene. J Med Genet 2006, 43: 148-152]