Kyselina vinná
Kyselina vinná (2,3-dihydroxybutandiová kyselina, kyselina dihydroxyjantarová, anglicky acidum tartaricum z řeckého tartaros - peklo, název kvůli hořlavosti a korozivním účinkům). Funkční vzorec je HOOC–CH(OH)–CH(OH)–COOH. Kyselina vinná je bezbarvá krystalická látka, dobře rozpustná ve vodě, kyselé chuti. Její soli se nazývají vinany.

| Kyselina vinná | |
|---|---|
 | |

Vzhled | |
| Obecné | |
| Systematický název | 2,3-dihydroxybutandiová kyselina |
| Triviální název | kyselina vinná |
| Ostatní názvy | 2,3-dihydroxyjantarová kyselina |
| Funkční vzorec | HOOCCH(OH)CH(OH)COOH |
| Sumární vzorec | C4H6O6 |
| Vzhled | bílý prášek |
| Identifikace | |
| Registrační číslo CAS | 87-69-4 (L(+)) 147-71-7 (D(−)) 147-73-9 (meso-forma)&Units=SI 526-83-0 87-69-4 (L(+)) 147-71-7 (D(−)) 147-73-9 (meso-forma) |
| Vlastnosti | |
| Molární hmotnost | 150,087 g/mol |
| Teplota tání | 169–170 °C (opticky aktivní) 142 °C (meso-forma) 206 °C (racemát) |
| Hustota | 1,759 8 g/cm³ (opticky aktivní) 1,666 g/cm³ (meso-forma) 1,788 g/cm³ (racemát) |
| Rozpustnost ve vodě | 133 g/100 ml (20 °C) |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Kyselina vinná byla vinařům známa po staletí. Již kolem roku 800 byla alchymistou Jabir ibn Hayyanem izolována ze své soli hydrogenvinanu draselného (vinný kámen). Ale až v roce 1769 vyvinul švédský chemik Carl Wilhelm Scheele proces pro její extrakci.
Tato přirozeně se vyskytující krystalická organická kyselina se nachází v mnoha druzích ovoce, zejména ve vinné révě, ale také v banánech, tamarindech a citrusech.
Její sůl hydrogenvinan draselný vzniká při výrobě vína. Kyselina vinná je proto jednou z hlavních kyselin ve víně, které určují její senzorické i další vlastnosti. V EU je schválena jako potravinářská přídatná látka E 334.
Chiralita
Historie
Důležitou roli při objevu chemické chirality hrála právě kyselina vinná. Tato její vlastnost byla poprvé pozorována v roce 1832 Jean-Baptiste Biotem, který objevil její schopnost otáčet polarizovaným světlem. V tomto výzkumu pokračoval Louis Pasteur a v roce 1847 zjistil, že krystaly vinanu sodno-amonného jsou také chirální. Při ručním tříděním různě tvarovaných krystalů Pasteur jako první vyrobil čistý vzorek kyseliny levovinné.
Optická aktivita
- Optická aktivita souvisí s vnitřním prostorovým uspořádáním atomů v molekule.
- Opticky aktivní látky stáčejí rovinu polarizovaného monochromatického záření doleva nebo doprava.
- Nejčastějšími opticky aktivními látkami jsou organické sloučeniny uhlíku.
Chirální molekuly
- Chirální molekuly obsahují asymetrický atom, který se nazývá chirální centrum molekuly. Dvojice takových molekul se k sobě chovají jako předmět a jeho obraz v zrcadle (nebo jako levá a pravá ruka). Tato jejich vlastnost se nazývá chiralita (z řeckého chiros, česky ruka nebo dlaň).
- Centrum chirality je atom, na který jsou ostatní atomy navázány zrcadlově asymetricky. Většinou se jedná o atom uhlíku se čtyřmi různými substituenty. Takový atom uhlíku se nazývá asymetrický uhlík.
Optické izomery
Dvojice látek, které obsahují asymetrický uhlík a vyskytují se ve dvou formách (předmět - obraz), se nazývají optické izomery (enantiomery nebo optické antipody).
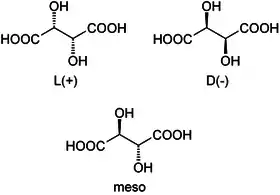
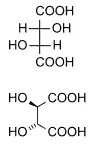
Příkladem takové opticky aktivní látky je kyselina vinná, která se vyskytuje ve třech optických izomerech:
- L-vinná kyselina (konfiguračně L-, opticky pravotočivá, odtud starší název kyselina pravovinná)
- D-vinná kyselina (Konfiguračně D-, opticky levotočivá, odtud starší název kyselina levovinná)
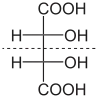
- meso-vinná kyselina (achirální sloučenina, která není opticky aktivní)
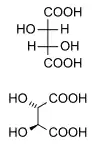
Směs stejných množství pravotočivé a levotočivé látky vytváří opticky neaktivní látku (racemát), která polarizační rovinu nestáčí. Právě takovou látkou je opticky neaktivní kyselina hroznová, což je směs stejných množství pravotočivé a levotočivé kyseliny vinné (molekuly kyseliny levovinné a pravovinné jsou svými zrcadlovými obrazy).
Výskyt
V přírodě je nejvíce rozšířena L-vinná kyselina a racemická kyselina vinná neboli kyselina hroznová. Je obsažena například ve vinných hroznech, ananasu, banánech, tamarindech a citrusech.
Kyselina vinná se obvykle získává jako vedlejší produkt z hroznů při výrobě vína. Při tomto procesu se k vinanu draselnému postupně přidává hydroxid sodný, poté kyselina sírová za vzniku kyseliny vinné.
Použití
- Kyselina vinná se používá především k úpravě kyselosti ovocných nápojů, vín, cukrovinek, želé, pekařských výrobků, ovocných šťáv, mražených mléčných výrobků.
- Je složkou některých potravinářských barviv.
- Jako kyselá složka je součástí prášku do pečiva,
- Používá se jako emulgátor regulující proces rosolovatění nebo jako zvlhčující látka.
- Má vlastnost vázat železnaté a měďnaté ionty, které katalyzují samovolnou oxidaci tuků, a tím může zabraňovat procesu žluknutí.
- Z kyseliny vinné je odvozen vinan sodno-draselný neboli Seignettova sůl KOOCCH(OH)CH(OH)COONa, která je součástí Fehlingova činidla sloužícího k důkazu redukujících sacharidů.
- Mezi důležité deriváty kyseliny vinné patří emetikum (vinan draselno-antimonitý, při vyšších dávkách dávidlo).
Nežádoucí účinky
Nejsou známy nežádoucí účinky kyseliny vinné, je považována za bezpečnou látku. V potravinách se vyskytuje jako přirozená složka. Ve velkém množství však může mít projímavé účinky nebo může způsobit zánět žaludku a střev. D-forma kyseliny vinné může při vylučování způsobit vznik a růst krystalů. Přijatelná denní dávka je 0-30 mg/kg tělesné hmotnosti.
Reference
V tomto článku byly použity překlady textů z článků Tartaric acid na anglické Wikipedii a Weinsäure na německé Wikipedii.
- Tartaric acid. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu kyselina vinná na Wikimedia Commons
Obrázky, zvuky či videa k tématu kyselina vinná na Wikimedia Commons  Galerie kyselina vinná na Wikimedia Commons
Galerie kyselina vinná na Wikimedia Commons Encyklopedické heslo Vinná kyselina v Ottově slovníku naučném ve Wikizdrojích
Encyklopedické heslo Vinná kyselina v Ottově slovníku naučném ve Wikizdrojích- Seznam děl v Souborném katalogu ČR, jejichž tématem je Kyselina vinná

