Nitrobenzén
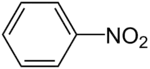
Nitrobenzén (zriedkavejšie nitrobenzol) je prudko jedovatá, mierne nažltlá kvapalina s charakteristickým zápachom. Racionálny vzorec nitrobenzénu je C6H5–NO2, nitroskupina je priamo viazaná na aromatickom jadre.

| Nitrobenzén | |
 | |
| CAS | 98-95-3 |
| Sumárny vzorec | C6H5NO2 |
| Mólová hmotnosť | 123,06 g/mol |
| Teplota topenia | −5,85 °C |
| Teplota varu | 210,9 °C |
| Hustota | 1199 kg/m3 (20 °C) |
| Index lomu | 1,553 (20 °C, 589 nm) |
| Teplota vzplanutia | 88 °C |
| Teplota samovznietenia | 480 °C |
| Tlak pár | 30 Pa (20 °C) |
| Rozpustnosť (voda) | 1,9 g/l vody (20 °C) |
| Skupenstvo | kvapalné |
Vlastnosti
Fyzikálne vlastnosti
Nitrobenzén je pri normálnych podmienkach bezfarebná resp. mierne nažltlá olejovitá kvapalina s charakteristickým horkomandľovým zápachom. Teplota topenia notrobenzénu je 5,85 °C, teplota varu 210,9 °C. Ostatné fyzikálne vlastnosti sú uvedené v tabuľke.
Chemické vlastnosti
Nitroskupina je zaujímavá najmä z hľadiska väzbových pomerov. Tradičná štruktúra tejto skupiny nie je uspokojivá, pretože atómy kyslíka majú v nej nerovnocenné postavenie.
Lepšiu predstavu o väzbách nitrobenzénu nám podáva delokalizácia elektrónov, čím sa obidva atómy kyslíka stanú rovnocenné.
Nitroskupina v molekule nitrobenzénu znižuje elektrónovú hustotu na aromaticom jadre (−M efekt), a preto prebiehajú elektrofilné substitučné reakcie pomerne ťažko, ale silnými nitračnými činidlami možno pripraviť aj trinitrobenzén.

V laboratórnej i priemyselnej praxi sa hojne využíva redukcia nitrobenzénu, pretože voľbou podmienok reakcie je možné dosiahnuť rôzne produkty: anilín, fenylhydroxylamín, hydrazobenzén, azoxybenzén. Najväčší význam má redukcia v kyslom prostredí, je to metóda priemyselnej výroby anilínu:
| Chemický portál |