Lanosterol-14α-demetyláza
Oxidačnú demetyláciu lanosterolu na cholestatrién katalyzuje lanosterol-14α-demetyláza, nazývaná tiež:
- lanosterol-14α-metyldemetyláza-cytochróm P450
- lanosterol-14α-metyldemetyláza
- 14α-metyldemethyláza.
14α-metylová skupina je prvá metylová skupina lanosterolu, ktorá sa odstráni pri premene lanosterolu na cholesterol. Jej odstránenie je nutné, aby získané steroly mohli plniť svoju membránovú a regulačnú úlohu. Substrátová špecifita enzýmu lanosterol-14α-demetyláza vyžaduje štruktúrne prvky, ktoré musí substrát obsahovať, aby mohlo dôjsť k jeho 14α-demetylácii:
- C3-hydroxylovú skupinu
- Δ8 dvojitú väzbu (dvojitú väzbu medzi C8 a C9)
- 14α-metylovú skupinu.
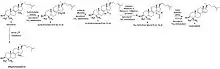
Lanosterol-14α-demetyláza je oxidoreduktáza, ktorá na premenu lanosterolu na cholestatrién vyžaduje tri molekuly NADPH a tri molekuly kyslíka O2, pričom iba jeden atóm kyslíka molekuly O2 skončí v cieľovej molekule. Druhý atóm kyslíka vytvorí molekulu vody H2O, čiže slúži ako akceptor elektrónov. Keďže redukcia dvoch atómov kyslíka v molekule O2 vyžaduje štyri elektróny, ďalšie dva elektróny na redukciu druhého atómu kyslíka poskytne substrát (zároveň sa tento redukovaný atóm kyslíka naviaže na molekulu substrátu). Z opísaného mechanizmu je jasné, že lanosterol-14α-demetyláza je monooxygenáza.
Lanosterol-14α-demetyláza katalyzuje tri následné monooxygenačné reakcie:
- premena lanosterolu na 3β-hydroxylanost-8-én-32-ol
- premena 3β-hydroxylanost-8-én-32-olu na 3β-hydroxylanost-8-en-32-ál
- premena 3β-hydroxylanost-8-en-32-álu na 14α-formyloxy-lanost-8-en-3β-ol
Pre poslednú oxidáciu bol navrhnutý mechanizmus zahŕňajúci atak karbonylovej skupiny peroxoskupinou, Bayerovu - Villigerovu reakciu (prešmyk).
Lanosterol-14α-demetyláza katalyzuje aj eliminačnú reakciu 14α-formyloxy-lanost-8-en-3β-olu na cholestatrién, čo je deformylácia za bázickej katalýzy.[1]
Inhibítory lanosterol-14α-demetylázy
Lanosterol-14α-demetyláza je inhibovaná lipofilnými imidazolmi, ako je mikonazol alebo ketokonazol, ktoré sa koordinujú pomocou dusíka imidazolového heterocyklu na hémové železo cytochrómu P450 lanosterol-14α-demetylázy, čím blokujú prístup molekuly kyslíka ku centrálnemu atómu železa. V dôsledku tejto inhibície sa začne hromadiť dihydrolanosterol, čo je produkt redukcie dvojitej väzby na bočnom reťazci lanosterolu, čo je reakcia katalyzovaná sterol-Δ24-reduktázou.[1]
Referencie
- RISLEY, John M.. Cholesterol Biosynthesis: Lanosterol to Cholesterol. Journal of Chemical Education, 2002-03, roč. 79, čís. 3, s. 377. Dostupné online [cit. 2021-03-11]. ISSN 0021-9584. DOI: 10.1021/ed079p377. (po anglicky)