Narasakova–Prasadova redukce
Narasakova–Prasadova redukce (někdy nazývaná jen Narasakova redukce) je diastereoselektivní organická redukční reakce β-hydroxyketonů za vzniku odpovídajících syn-diolů; přitom se používají chelatační činidla založená na boru, například BBu2OMe, a redukční činidla, nejčastěji borohydrid sodný. Poprvé byla tato reakce popsána v roce 1984.[1]
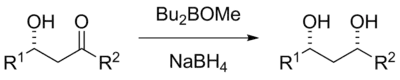
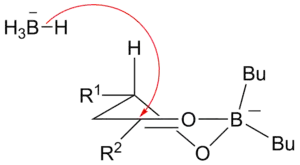
Meziproduktem je níže zobrazený šestičlenný přechodný stav. Chelatace organoboranem vyvolá přesun hydridu z vrchní strany, protože tím, podle Fürstova-Plattnerova pravidla, vzniká stabilnější židličkovitá konformace produktu. Poté proběhne mezimolekulární přesun hydridu z NaBH4 jako axiální atak z opačné strany vzhledem k alkoholu.[1]
Podobnou reakcí je Evansova–Saksenaova redukce, při níž se používá jiný organoboranový reaktant, aby proběhl vnitromolekulární přesun hydridu na stejné straně alkoholu a vytvořil se anti-diol.
Narasakova–Prasadova redukce byla zařazena do mnoha totálních syntéz,[2] například u diskdermolidu.[3]
Reference
V tomto článku byl použit překlad textu z článku Narasaka–Prasad reduction na anglické Wikipedii.
- Jaemoon Yang. Six-Membered Transition States in Organic Synthesis. [s.l.]: John Wiley & Sons, 2008. Dostupné online. ISBN 9780470199046. Kapitola Diastereoselective Syn-Reduction of β-Hydroxy Ketones, s. 151–155.
- Henning Priepke; Stefan Weigand; Reinhard Brückner. A Butyrolactone → 1,3-Diol Strategy for the Obtention of Tolypothrix Polyethers – Stereoselective Synthesis of a Key Lactone Precursor. Liebigs Annalen. 2006, s. 1635–1644. DOI 10.1002/jlac.199719970804.
- Stuart Mickel; Daniel Niederer; Robert Daeffler; Osmani Adman; Ernst Kuesters; Emil Schmid; Karl Schaer. Large-Scale Synthesis of the Anti-Cancer Marine Natural Product (+)-Discodermolide. Part 5: Linkage of Fragments C1-6 and C7-24 and Finale. Organic Process Research & Development. 2004, s. 122–130. DOI 10.1021/op034134j.