Iontová vazba
Iontová vazba (heteropolární) je druh vnitromolekulární chemické vazby, která vzniká v případě, že rozdíl elektronegativit atomů účastnících se vazby, přesahuje 1,67[zdroj?]. Potom dochází k tomu, že jeden atom k sobě přitáhne od druhého atomu elektron příp. více elektronů, který potřebuje k dosažení stabilní elektronové konfigurace a stane se záporným iontem (aniontem); druhý atom se po jeho/jejich ztrátě stane kladným iontem (kationtem). Následně jsou atomy k sobě vázány především díky elektrostatické přitažlivé síle, jež působí mezi částicemi s opačným nábojem. Kromě toho má iontová vazba úzký vztah k polarizované kovalentní vazbě a to jako její extrémní případ, který je kvalitativně odlišný od normální varianty této vazby.
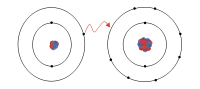
Typickou vlastností sloučenin s iontovou vazbou je jejich dobrá rozpustnost ve vodě. Rozpouštění těchto sloučenin ve vodě probíhá jejich disociací (rozpadem) na ionty, z nichž jsou složeny.
Příklady vzniku iontové vazby:
- Li + F → Li+F−
- 3Na + N → Na +
3 N3−
Nejsilnější iontová vazba se vyskytuje u solí kovů.