Adice
Adice je reakce, při které dochází k zániku π vazeb (násobných vazeb) nebo otevření cyklické molekuly a dochází k navázání skupiny či atomu sigma vazbou. Z jedné dvojné vazby tedy vznikají dvě jednoduché. Na násobnou vazbu jedné molekuly se aduje molekula druhá.
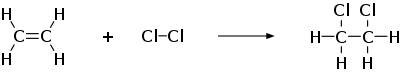
Typický příklad adice: chlorace ethenu
Opakem adice je eliminace, kdy odštěpením atomů (nebo skupin atomů) vznikne násobná vazba nebo dojde k uzavření cyklu.
Pravidla pro adici
Kharaschovo pravidlo
- Při radikálové „adici“ na alkeny se kladnější část činidla vlivem vnějších podmínek (UV záření, přítomnost radikálů) „aduje“ na uhlík s menším počtem vodíků.
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.